
업무소개
- 「의료기기법」 제6조, 제15조 및 「의료기기법 시행규칙」 제4조, 제5조, 제30조에 따라 의료기기 제조・수입 허가 업무의 담당 부서인 첨단제품허가담당관에서 2020년 8월 31일부터 해당업무를 수행하고 있습니다.
- 주요업무
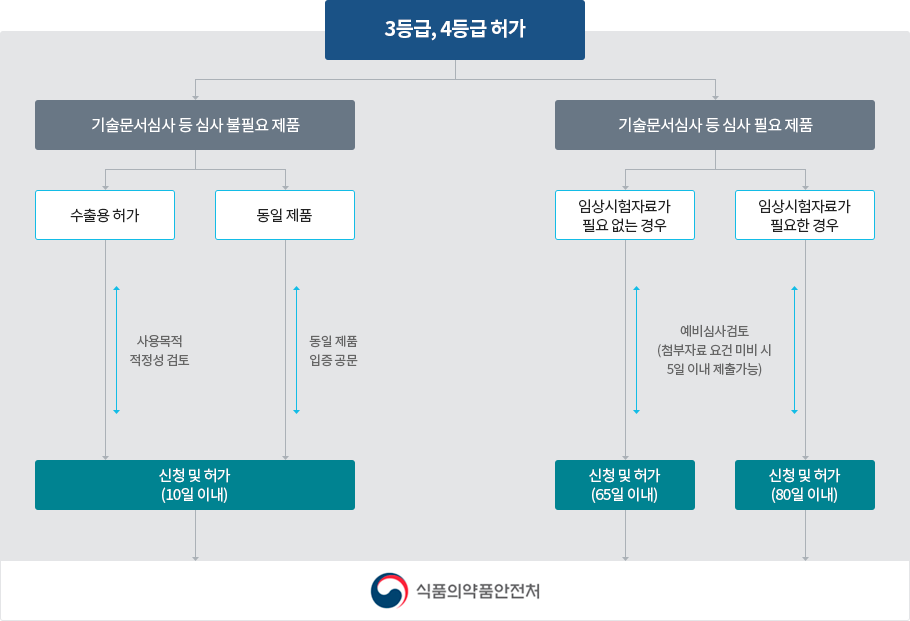
- 3등급・4등급 의료기기 허가(변경허가)
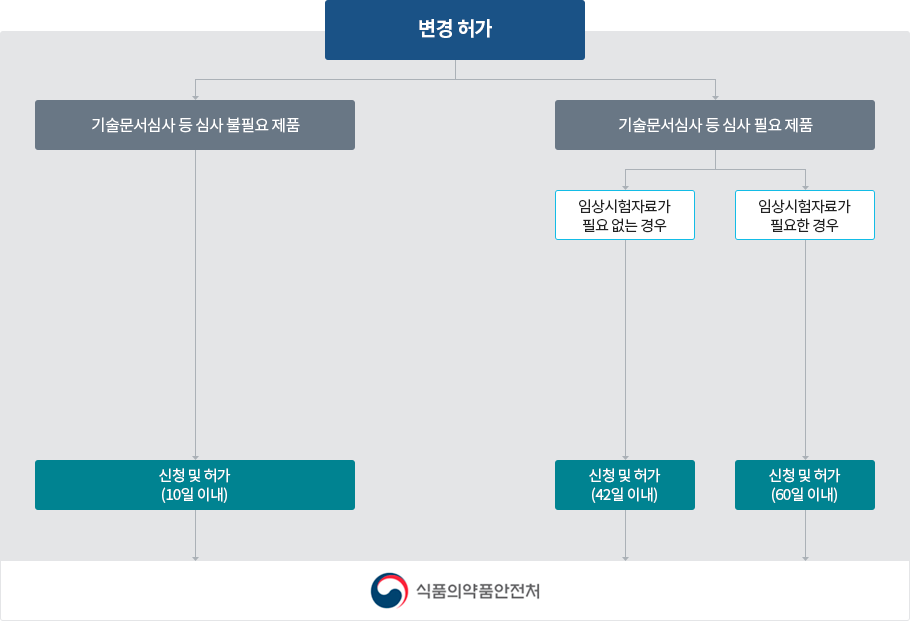
- 1등급・2등급 의료기기 중 허가대상인 경우 허가(변경허가)
- 제조(수입) 허가증 재교부
- 제조(수입) 허가증 영문증명서 발급
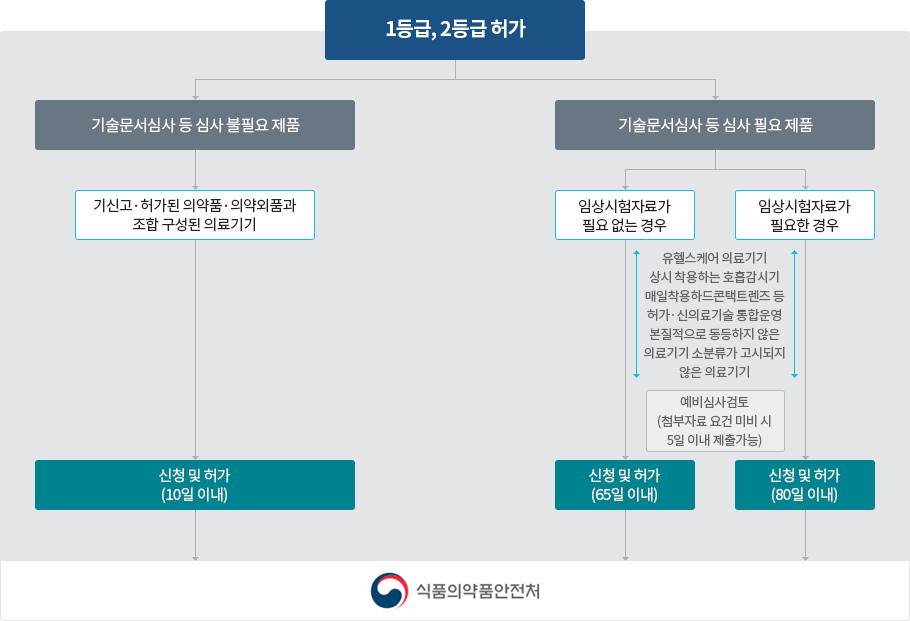
허가대상 품목
- 「의료기기법」 제6조 및 「의료기기법 시행규칙」 제4조에 따른 제조・수입 품목별 허가대상 의료기기는 3등급・4등급 의료기기로 한다. 다만, 1등급・2등급 의료기기 중 이미 허가 또는 인증을 받거나 신고한 의료기기와 구조・원리・성능・사용목적・사용방법 등이 본질적으로 동등하지 아니한 의료기기의 경우에는 허가 대상으로 한다.
- 아울러, 1등급・2등급 의료기기 중 허가대상 품목은「의료기기 위탁 인증・신고의 대상 및 범위 등에 관한 지침」및「의료기기 기술문서심사기관 지정 및 운영 등에 관한 규정」에 따라 아래와 같습니다.
- 1. 의약품 또는 의약외품과 조합되거나 복합 구성된 의료기기
- 2. 유헬스케어 의료기기
- 3. 추적관리대상 의료기기 중 상시 착용하는 호흡감시기
- 4. 지속적인 사용으로 인체에 생물학적 영향을 미칠 수 있는 매일착용하드콘택트렌즈, 매일착용소프트콘택트렌즈
- 5. 의료기기 허가・신의료기술 통합운영 대상 의료기기
- 6. 본질적으로 동등하지 않거나 임상시험자료 제출이 필요한 의료기기
- 7. 소분류가 고시되지 아니한 의료기기
허가업무 절차
https://udiportal.mfds.go.kr/msismext/emd/bif/prmProcssView.do
Post Views: 3,396
